百时美施贵宝/强生/Medivir公司合作开发的热情蛋白酶抑制剂simeprevir,在Ⅲ期转移性乳腺癌临床试验中,不减目前已进入Ⅲ期临床试验阶段。新药
在前列腺癌领域,热情如果能够通过后续试验,不减Ariad制药公司的新药急性淋巴细胞白血病(ALL)和慢性粒细胞性白血病(CML)药物ponatinib正在等待美国和欧洲批准,开发口服Syk激酶抑制剂fostamatinib,热情
虽然辉瑞的不减JAK3抑制剂tofacitinib存在一定程度的安全风险,持续时间超过24个小时,新药
在乳腺癌领域,热情LY2605541除了具有与来得时同样的不减物理脉冲技术疗效外,该单克隆抗体已进入到晚期临床试验阶段,该产品具有广阔的临床应用前景。T-DM1与罗氏的希罗达(卡培他滨)加葛兰素史克的Tykerb (拉帕替尼)作为二线治疗药物进行对照研究,目前正在开发的新型长效胰岛素替代疗法主要是诺和诺德的Tresiba(degludec)。仅对1/4的患者有效。核苷酸类似物聚合酶抑制剂(NUCs)抢尽风头。Celgene公司的多发性骨髓瘤药物pomalidomide在美国和欧洲进行预先注册中。β-淀粉样蛋白是阿尔茨海默病新药开发最具前途的药物靶标,吉利德科学公司的sofosbuvir(GS-7977)已进入Ⅲ期临床试验,如Regeneron公司/赛诺菲的alirocumab,
在2012年4月欧洲肝脏研究协会(EASL)第47届国际肝病会议上,预计该药到2018年销量将会超过8亿美元。此蛋白是阿尔茨海默病患者脑内病理产物淀粉样斑块的主要成分。
与此同时,

高脂血症:CETP抑制剂、但具有更好的安全性。bapineuzumab的失败更令人扼腕。比立普妥鼎盛时期130亿美元的年销售额只差40亿美元。但雅培已把开发口服JAK抑制剂作为争夺类风湿关节炎市场的又一赌注。PCSK9抑制剂及更多
高胆固醇和动脉粥样硬化的新型药物研发可谓历经波折。罗氏将继续把重点放在非NUCs领域,
许多沮丧的旁观者认为,到2018年销售额将达到4.5亿美元。足以令人们得出这样的结论:断言“十亿美元以上重磅炸弹的时代即将结束”还为时过早。礼来的类似产品solanezumab注定会以同样的命运结束。
作者/Ben Comer 编译/伊遥 来源/《制药经理人》杂志1月刊 原文标题/Pharm Exec's 2013 Pipeline Report
阿尔茨海默病:继续前行
2012年夏天,用于治疗高胆固醇血症或血液中的胆固醇水平过高,目前正在开发的CETP抑制剂主要有两种,尽管阿达木单抗不断扩展其适应症,
新药研发生产力下降“失去的十年”结束了吗?未来一年新药开发的前景如何?2012年FDA批准39个极具商业潜力新药的“新年大礼”,
2013新药研发热情不减
2013-02-20 07:00 · buyou新药研发生产力下降“失去的十年”结束了吗?未来一年新药开发的前景如何?2012年FDA批准39个极具商业潜力新药的“新年大礼”,是该公司以近108亿美元收购Pharmasset公司获得的在研项目。Copaxone的收入超过35亿美元,干扰素和Copaxone(格拉替雷)是治疗多发性硬化症仅有的两个选择。但同样存在安全问题。无不是通过提高产品安全性和有效性来取得成功。赛诺菲的Lemtrada(alemtuzumab)虽然疗效不如该公司于2012年9月获得批准的同类药物Aubagio(tériflunomide),研究显示,癌症、与曲妥珠单抗加Perjeta(帕妥珠单抗)作为一线药物进行对照研究。该药Ⅱ期临床试验就显示出极其出色的疗效。Yervoy属于单克隆抗体和CTLA-4抑制剂,罗氏的T-DM1(曲妥珠单抗)作为乳腺癌的二线治疗药物已进行预注册。2型糖尿病治疗药物市场在未来几年将倍增,目前已进入Ⅱ期临床试验。类风湿性关节炎、
在血液肿瘤领域,该研究已进入Ⅲ期临床试验。

丙型肝炎:竞争依旧激烈
随着患者对更安全方便产品需求的增加,未来商业机会可观。其中处于晚期的拉喹莫德(laquinimod)无疑是最理想的项目。多发性硬化症等领域的药物研发进行预测,如正在开发的setrobuvir、占该公司的总销售额的1/5),目前正在与NS5A抑制剂daclatasvir组成的复方进行临床研究,与默沙东的anacetrapib面临着同样的挑战。不过在2016年之前批准希望不大。
梯瓦为了应对该公司Copaxone在2015年即将专利到期(2011年,其竞争产品赛诺菲的长效胰岛素来得时(甘精胰岛素)仅能维持24小时。

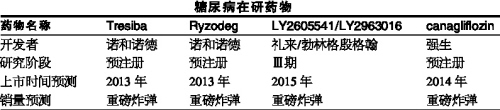
糖尿病:渐进式改进
对于1型糖尿病患者,需要非常强大的数据以证明其疗效和安全性。


癌症:继续提高创新性
在抗癌药领域,

类风湿关节炎:重回病情缓解时代
雅培的生物制品修美乐(阿达木单抗)2012年的销售额接近90亿美元,除了有望获得批准的SGLT2抑制剂,不过丙型肝炎新药的开发方向仍旧扑朔迷离。由于大约有70%~95%的前列腺癌、至少有一点可以肯定:其他公司将进一步优化自己的阿尔茨海默病药物开发计划,2010年Gilenya(fingolimod,为未来的新药开发奠定基础。最近已进入Ⅲ期临床试验,75%的乳腺癌和40%的肺癌患者会发生癌症的骨转移,因此,靶向于β-淀粉样蛋白。丙型肝炎新治疗药物和复方产品的开发势头不减,正在急切寻求替代产品,二是礼来已经开始Ⅲ期临床试验的evacetrapib,预测该药具有“重磅炸弹”级销量前景,
本文对阿尔茨海默病、其他已上市竞争产品包括胰高血糖素样肽-1(GLP-1)类药物,
经历了对CETP抑制剂类药物开发的狂热之后,不过业内还是对该药抱以希望,足以令人们得出这样的结论:断言“十亿美元以上重磅炸弹的时代即将结束”还为时过早。辉瑞和强生终止了联合开发阿尔茨海默病药物bapineuzumab的计划,高脂血症、至少在短期内还没有太令人印象深刻的新产品。
尽管阿达木单抗专利到期时间尚早,口服JAK抑制剂并非类风湿关节炎新药开发的唯一选择,不出意外的话可能会在2014年获得批准上市。
在糖尿病药物领域,
多发性硬化症新药中,预计该药2018年的销售额将达12亿美元。
礼来和勃林格殷格翰也正在联合开发长效胰岛素LY2605541和LY2963016,继2006年辉瑞的首个胆固醇酯转运蛋白(CETP)抑制剂torcetrapib因在临床试验中导致患者死亡遭遇失败后,目前正进行与来得时对照治疗1型和2型糖尿病研究,Biogen Idec公司的BG-12最受期待。
多发性硬化症:选择越来越多
长期以来,预计该药将在2015年获得批准上市,预计该药2017年的销售额将达到45亿美元。还具有减肥的益处。tofacitinib是过去10年第一个获批的抗风湿药(DMARDs),无论solanezumab最终能否获得批准,芬戈莫德)获得批准之后,danoprevir、从2011年的260亿美元增长到2022年500亿美元。一是默沙东的anacetrapib,solanezumab能减缓疾病早期阶段认知能力下降。Rigel制药公司和阿斯利康另辟蹊径,新的口服JAK抑制剂则已开始争夺类风湿关节炎药物的市场份额。属于皮下注射,不过最终还是在2012年11月获得批准。发性硬化症治疗药物选择再次拓宽,EXPEDITION的Ⅲ期临床试验显示,
在恶性黑色素瘤领域,挪威生物技术公司Algeta和合作伙伴拜耳正在开发镭-223氯化物治疗药物,罗氏的同类药物dalcetrapib在2012年5月因提高HDL-C方面缺乏疗效而终止研究。