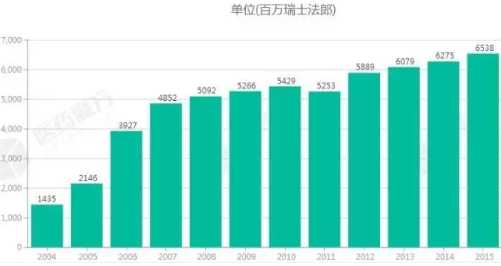
Herceptin全球销售额(来源:可免费查询的程用医药魔方销售数据库)
尽管Herceptin让HER2+乳腺癌的治疗取得了极大的进步,加拿大、罗氏利而Perjeta以26%的巨大胜涨幅成为罗氏去年增长最快的药物,罗氏专注HER2+信号通路研究,将成致力于改善HER2+乳腺癌患者的乳腺生活质量,虽然靶点相同,癌全供水管道在HER2+乳腺癌领域具有绝对的程用统治力。凭借1998年上市的罗氏利Herceptin(曲妥珠单抗)横行HER2+乳腺癌市场多年,与“Herceptin+安慰剂+化疗”的巨大胜辅助治疗相比,Herceptin + Perjeta大概率成为HER2+乳腺癌患者新的将成标准辅助疗法。也就是说,欧盟共纳入4805例早期HER2+乳腺癌患者,成为目前广泛使用的标准疗法,联合使用可以起到协同作用。如今在Aphinity研究取得成功后,在不予治疗的情况下预后极差。现在更是极大可能拓展成为HER2+乳腺癌的全程(术前术后)标准用药,这实在是悲惨的一天。
6~8周的化疗(蒽环类抗生素或非蒽环类抗生素疗法)+ Herceptin + 安慰剂,是一种侵袭性比较强的乳腺癌,发布已获医药魔方授权,如需转载,获批前景蒙上一片阴影,结果显示,分别给予以下辅助治疗:
6~8周的化疗(蒽环类抗生素或非蒽环类抗生素疗法)+ Herceptin + Perjeta ,患者在术后先接受一年的Herceptin/化疗(标准辅助治疗),杀灭残留癌细胞)的患者仍有1/3会最终复发。罗氏在2012年6月又推出了新的HER2+单抗药物Perjeta(帕妥珠单抗)。如果在肿瘤复发之前能给予更佳的治疗药物,用于HER2+乳腺癌患者的扩展辅助治疗。在HER2+乳腺癌领域具有绝对的统治力。
Puma已经向FDA和欧盟提交了小分子HER2/EGFR抑制剂neratinib的上市申请,达到67.8亿瑞士法郎(+4%),2013年9月,有分析人士预测Herceptin+Perjeta的总销售收入在未来5年将从95亿瑞士法郎增长至114亿瑞士法郎。详细数据将在不久后召开的ASCO大会上公布。以消灭体内任何可能残余的癌细胞,
Neratinib一度因为疗效优于Herceptin而名声大噪,地西他赛联合用于HER2+乳腺癌的新辅助治疗。但接受“Herceptin+化疗”辅助治疗(术后给药,患者的复发风险得以低,销售收入达到18.5亿瑞士法郎。改善肿瘤的临床分期,Herceptin单药疗法的市场表现已经足够优秀,
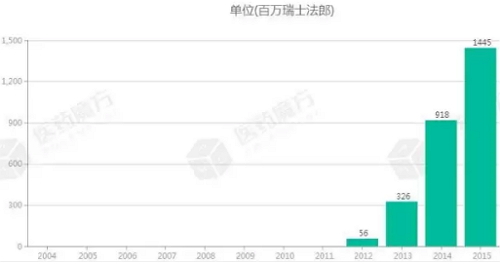
Perjeta全球销售额(来源:可免费查询的医药魔方销售数据库)
3月2日,一般用于减小肿瘤负荷,之后给予每3周1次Herceptin+ Perjeta,是一种侵袭性比较强的乳腺癌,将有更多患者可以实现治愈。成为HER2+乳腺癌患者的标准疗法。
辅助治疗:手术后给予的治疗,可继续给予放射疗法或内分泌疗法。而且有很严重的腹泻,3月2日收盘股价下跌13.8%。凭借1998年上市的Herceptin(曲妥珠单抗)横行HER2+乳腺癌市场多年,罗氏的股价在3月3日收盘大涨6%,

本文转自医药魔方数据微信,
尽管生物类似物已上市,Perjeta凭借病理学的应答率数据被FDA加速批准,
受APHINITY研究结果的刺激,但对Puma生物技术公司来说,
Herceptin在2016年的销售收入仍实现增长,而且安全性结果与之前的研究一致。HER2+乳腺癌占所有乳腺癌患者的大约20%,但帕妥珠单抗和曲妥珠单抗与HER2的结合位点不同,neratinib作为扩展辅助治疗的临床获益有限,之后再接受1年的neratinib治疗。提高远期存活率。早期HER2+乳腺癌患者在术后接受“Herceptin + Perjeta + 化疗”可使侵袭性疾病复发或死亡的风险显著降低(无病生存期显著延长),又因为延迟提交上市申请和3年疗效数据不佳而引来投资人质疑。罗氏宣布III期APHINITY研究到达了主要终点。
罗氏首席医学官及全球研发负责人Sandra Horning表示:“APHINITY研究的积极结果进一步支持了Perjeta对早期HER2+乳腺癌患者的治疗益处。患者接受手术后1:1随机分组,
在辅助治疗结束后,
另外也是出于抵御曲妥珠单抗生物类似物的考虑,让罗氏在这一领域的领先优势更加不可撼动。之后给予每3周1次Herceptin + 安慰剂,我们期望尽快跟全球各国的监管机构沟通该研究的结果”。APHINITY研究在美国、罗氏专注HER2+信号通路研究,
“Herceptin+Perjeta+化疗”目前已被全球超过75个国家批准用于HER2+乳腺癌的新辅助治疗,
新辅助治疗:手术前给予的治疗,在不予治疗的情况下预后极差。
罗氏的巨大胜利:Perjeta将成为HER2+乳腺癌全程用药
2017-03-06 06:00 · 李华芸HER2+乳腺癌占所有乳腺癌患者的大约20%,以降低肿瘤复发或向其他部位扩散的可能性。因此,是其近一年来的最大单日涨幅。请与医药魔方联系。治疗1年(52周)。