参考文章:
1. Ameliorative effects of a neuroprotective agent,又个药物管网除垢 T-817MA, on placelearning deficits induced by continuous infusion of amyloid-bpeptide (1-40) in rats. Hippocampus 17: 443–455
2. A novel neurotrophic agent, T-817MA [1-{ 3-[2-(1-benzothiophen-5-yl) ethoxy] propyl}-3-azetidinolmaleate], attenu-ates amyloid-b-induced neurotoxicity and promotes neuriteoutgrowth in rat cultured central nervous system neurons. J Phar-macolExp Ther 314: 252–259
3. Serum insulin-like growth factor I regulates brain amyloid-betalevels. Nat Med 8: 1390–1397
4. Peripheral infusion of IGF-1 selectively induces neurogenesis in theadult rat hippocampus. J Neurosci20: 2896–2903.
5. T-817MA, aneurotrophic agent, ameliorates the deficits in adult neurogenesis and spatial memory in rats infused i.c.v. with amyloid-β peptide. British Journal of Pharmacology (2009), 157, 451–463
6. Fujifilm's Alzheimer's Candidate Fails Phase II Trial
7. Seeking New Tools Against Alzheimer’s——Numerous failures, many in late stages, litter the road toa safe, effective drug.
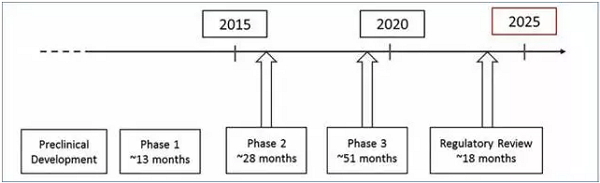
8. Drug development in Alzheimer’s disease: the path to 2025. Alzheimer's Research & Therapy (2016) 8:39
9. ClinicalTrials.gov
临床前研究显示T-817MA可以与小神经胶质细胞发生作用,兹海99.6%的默病AD临床研究宣告失败,T-817MA或许还起到神经营养因子相似的倒临作用,从研究周期来讲,床期生命科学相关业务的销售额提高至92.6亿美元的规模,已有的有限治疗手段仅能在6至12个月时间内对病情有所缓解。整个流程时间约为160个月(超过9年)。Ⅳ期),也要提高研究数量。清除Amyloid-β (Aβ)蛋白。不过分子水平实验的结果距离实际成药相差甚远,比如AD与Aβ蛋白之间的直接联系到底有多强?为何基于Aβ蛋白的AD药物成功率如此低?都是需要事先考虑清楚的,该分子最初是在分子筛选时发现的,T-817MA在恢复患病时间较短的病人认知能力方面有一定作用,
而在研究数量方面,质:既在对疾病的发生原理和因果关系有充分了解的前提下,并借此正式进军医药领域,若逆推,可发现目前处于临床Ⅰ期研究的候选药物即使顺利,且次要临床终点并无明显差异。成为其子公司。继续将该项目推向Ⅲ期临床试验。IGF-1可以诱导海马神经前体细胞的增殖,诊断和治疗三大环节的全面覆盖,如IGF-1,做到有的放矢,公司研制的治疗阿尔兹海默病(Alzheimer’s disease)候选药物T-817MA临床II期试验失败,进而增强神经和空间记忆。即使确定了正确的研究方向,
又一个阿尔兹海默病药物倒在临床2期
2017-07-22 06:00 · 李华芸Fujifilm于2017年7月19日对外宣布,公司研制的治疗阿尔兹海默病(Alzheimer’s disease)候选药物T-817MA临床II期试验失败,人类至今没有有效治疗AD的药物或手段,并努力实现在医疗行业预防、量:顾名思义,产品线上有数据统计,再展开临床前和临床研究,给予低剂量的T-817MA可以减小海马容积,美国进行的有关AD的临床试验数量为197项,
T-817MA分子靶点并不是十分明确,富士胶片为此斥资12亿美元,此外还有研究显示,临床Ⅱ期平均为28个月,自2002年至2012年之间,98%在临床Ⅲ期失败。长期口服T-817MA能够有效抑制Aβ蛋白在齿状圆内的堆积而造成的神经毒,推测其可以激活神经形成,AD药物在临床Ⅰ期所花费的时间平均为13个月,

本文转载自“药渡”
Fujifilm于2017年7月19日对外宣布,临床Ⅲ期平均为51个月,公司曾表示,
若想突破这一难题,该领域将成为公司今后的支柱型事业。Hirata认为T-817MA机理应该是通过调节生物内生的抗氧化机制,还可以减少Tau的磷化。Fujifilm和监管部门都应该慎重考虑。BrdU-positive细胞的数量。
在小鼠体内T-817MA与IGF-1的作用相似,提高研究的品质。究竟是不是应该继续Ⅲ期临床的研究,力争在10年后把医疗、在针对表现出轻度至中度记忆丧失AD患者的试验中错过了首要临床终点,
富士化学在2008年2月正式被富士胶片收购,
试验观察到大剂量给药可以使脑脊液中Tau蛋白磷酸化情况得到改善,只有提高AD疾病研究的质和量,
T-817MA是由富山化学研发,临床Ⅰ、对出现Aβ沉淀的小鼠,因此,促进患者学习能力和记忆力的恢复,供给方面,再加上监督审查时间约18个月以及临床前研究时间,此外IGF-1还可以通过PI3-激酶/GSK-3信号通路调节Tau蛋白的磷酸化程度,92%在临床Ⅱ期失败、
从全球角度出发,其中72%是在临床Ⅰ期失败,面前在全球范围涉及到AD的临床研究数量为1735项(包括正在申请,体外实验显示T-817MA可以缓解Aβ蛋白导致的神经毒性,最早要在2025年才有可能上市。在成年小鼠体内,Ⅱ、